疗效优异!再鼎医药ASCO发布DLL3 ADC产品数据
作者:生物制药进展杂评

1、在本年度ASCO中报道的ZL-1310主要临床数据
2、DLL3 靶点主要竞争格局双抗/三抗对决ADC/RDC
3、DLL3 核心产品临床数据比较,ZL-1310优势显著
4、DLL3 市场价值,过往交易大单频出,ZL-1310未来可期
2025年6月2日,再鼎医药在2025年ASCO(美国临床肿瘤学会)年会的壁报展示环节中,公布了正在进行的全球1a/1b期临床研究(NCT06179069)的更新数据。
该研究评估了公司的ADC新药zocilurtatug pelitecan(ZL-1310,靶点为DLL3),用于广泛期小细胞肺癌(ES-SCLC)患者的更新数据。此次公布的数据包括单药治疗剂量递增部分的更新结果,以及首次公布的来自6个剂量组总共89例入组患者的剂量扩展数据。
1、在本年度ASCO中报道的ZL-1310主要临床数据如下:
ZL-1310,采用可裂解linker,payload为拓扑异构酶I抑制剂,DAR值为8。
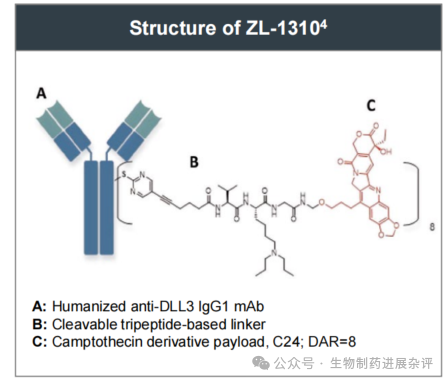
1.1 临床主要有效性结果
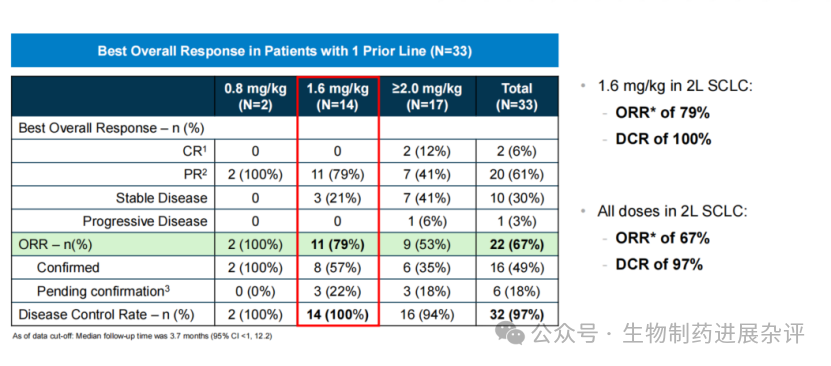
在2L治疗中,所有剂量组(n=33)患者的未确认客观缓解率(uORR)为67%,DCR为97%。1.6mg/kg剂量组(n=14)显示出最佳的疗效与耐受性组合,ORR为79%,DCR达100%。
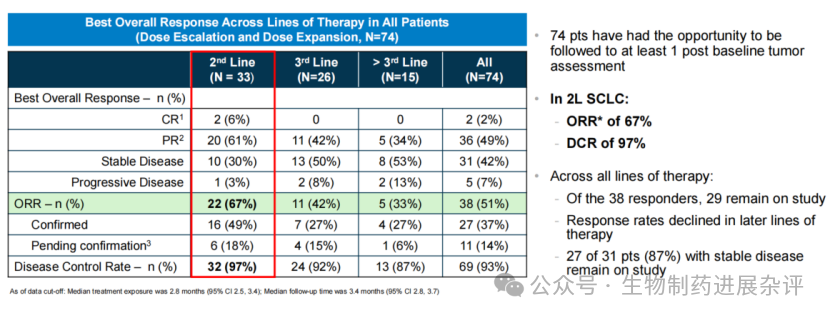
在所有剂量水平和治疗线数中(n=74),38例经确认(n=27)和未经确认(n=11)的客观缓解(ORR)的患者中,29例(76%)仍在接受治疗,其中时间最长的缓解者接受治疗已超过9个月。89%的患者肿瘤负荷减轻。
31例疾病稳定的患者中,27例(87%)仍在接受治疗。
随着患者既往治疗线数增加和剂量水平升高,缓解率呈现下降趋势,这与疾病更晚期及2.0mg/kg以上剂量可能的耐受性限制一致。
在治疗中,脑部转移患者仍有显著的治疗获益:在22例基线存在脑转移且疗效可评估的患者中,观察到68%的客观缓解率(ORR)。未接受过颅脑放疗的患者的ORR达86%。
在DLL3双特异性抗体经治,接受过不同线数治疗的患者中,观察到了治疗缓解。
中位随访时间尚未成熟,为3.4个月,因此中位缓解持续时间尚无法评估。
1.2、关键安全性数据
ZL-1310持续表现出良好的耐受性:
在<2.0mg/kg的剂量组中,3级及以上TRAEs发生率为6%(3),严重TRAEs发生率为4%(2)。
最常见的TRAEs为贫血(≥3级2%)和中性粒细胞减少(≥3级4%)。
未出现治疗终止情况,也未发生≥3级的间质性肺病(ILD)。
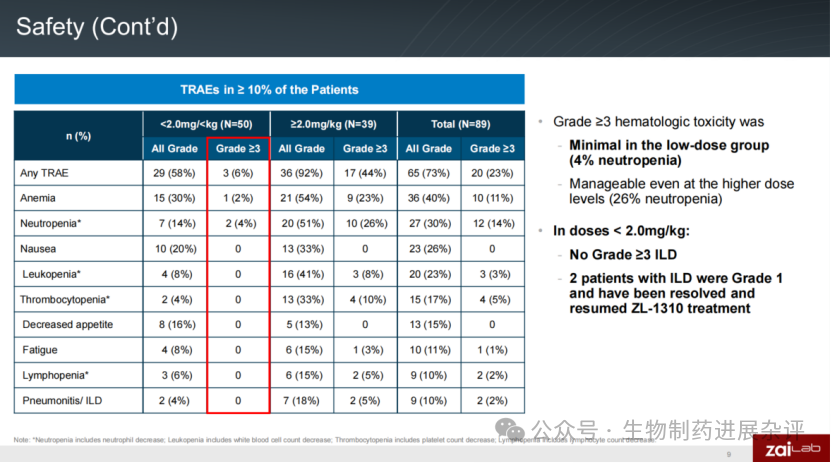
在所有剂量组中,3级及以上TRAEs发生率为23%,严重TRAEs为21%。最常见的TRAEs为贫血(≥3级11%)和中性粒细胞减少(≥3级14%)。
共出现5例因TRAEs导致的治疗终止,均发生在较高剂量组。报告了2例≥3级治疗相关ILD,分别出现在2.0mg/kg和2.4mg/kg剂量组。
综合评估1.6mg/kg剂量组显示出最佳的疗效与耐受性组合,因此只有在高剂量出现的导致治疗终止的TRAEs不会影响到未来临床应用,也为即将启动的关键注册性3期试验提供了明确的“最佳生物剂量”方向。
2、DLL3 靶点主要竞争格局双抗/三抗对决ADC/RDC
目前DLL3靶点有一个上市产品——Tarlatamab,十余个临床阶段产品,主要药物类型有:DLL3/CD3双抗/三抗产品共8个、4个ADC产品和3个RDC产品。
在4款ADC药物中再鼎医药的ZL-1310进度最快。
在总体的竞争中目前主要是ADC药物和双抗/三抗产品之间的竞争。
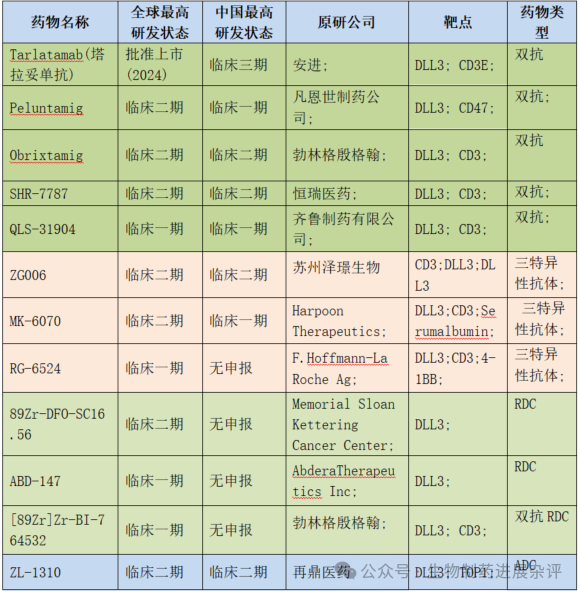
3、DLL3 核心产品临床数据比较,ZL-1310优势显著
在本年度ASCO上公开数据的主要有泽璟生物的ZG006、安进的Tarlatamab、BI的Obrixtamig和再鼎的ZL-1310,前三个为双抗/三抗产品,ADC产品仅有ZL-1310。
由于DLL3靶点目前主要适应症聚焦在小细胞肺癌领域,在该领域中B7-H3靶点的ADC产品同样值得关注,主要有:第一三共的Deruxtecan和明慧药业的MHB088C。数据总结如下:
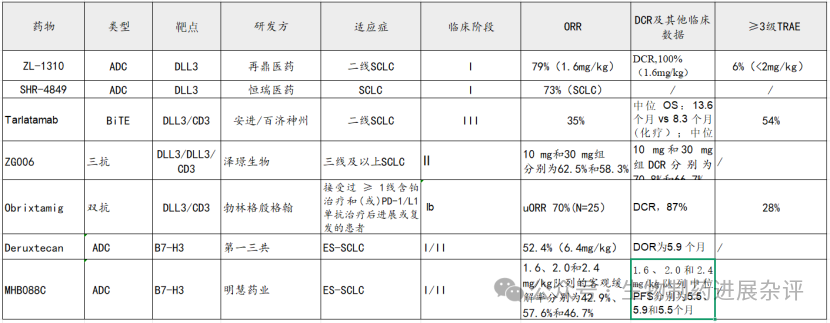
数据来源:根据公开数据整理
目前在DLL3靶点和小细胞肺癌领域,几款重要产品均公开了各自已取得的临床数据。由于产品类型不同,甚至靶点不同,因此在临床设计、入组患者基线/剂量等方面也各有差异。
尽管不能进行严谨的比对,但是通过这些数据,我们可以发现ZL-1310的ORR和可比的DCR数据均显示了未来成为临床获益最优产品的潜力。在安全性方面,在<2.0mg/kg的剂量组中,3级及以上TRAEs发生率为6%,意味着未来在临床应用中ZL-1310具有更高的安全性。
综合已经公开的有效性和安全性数据,ZL-1310具备成为同靶点领域中最优产品的潜力,未来值得期待。
4、DLL3 市场价值,过往交易大单频出,ZL-1310未来可期
Tarlatamab 是DLL3靶点唯一一个上市的产品,在美国上市时间为2024年5月,2024年全年实现销售额1.14亿美元。上市第一个半年销售额就突破1亿美元,表现还是很亮眼。
在过去的一年中,DLL3靶点在BD交易市场上也是十分活跃,共有5笔交易,其中两笔处于I期临床阶段的ADC产品的交易,交易总额均超过10亿美元。
试想一下,ZL-1310已经展示了如此亮眼的临床数据,而且在ADC产品中临床进度最快,如果达成交易,很可能是10亿美元级以上的交易~
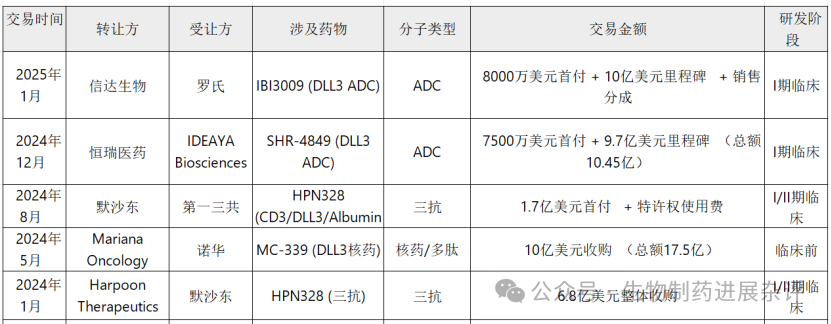
5、写在最后
ZL-1310在开发中一直不缺乏国际化的视野,再鼎从一期临床研究就开始进行全球临床研究,并保持了和FDA的充分沟通,在注册事务上无疑具有先发优势。从ZL-1310今年连续获得的孤儿药资格认定和快速审评资格认定就可见一斑。这为未来申请FDA的加速审评(AA)和申报上市,奠定了良好基础。再鼎医药一直以来的国际化视野和团队,ZL-1310未来的全球化之路很值得期待。
以上内容与数据,与有连云立场无关,不构成投资建议。据此操作,风险自担。
交易商排行
更多- 监管中EXNESS10-15年 | 英国监管 | 塞浦路斯监管 | 南非监管92.42
- 监管中FXTM 富拓10-15年 |塞浦路斯监管 | 英国监管 | 毛里求斯监管88.26
- 监管中axi15-20年 | 澳大利亚监管 | 英国监管 | 新西兰监管79.65
- 监管中GoldenGroup高地集团澳大利亚| 5-10年85.87
- 监管中Moneta Markets亿汇澳大利亚| 2-5年| 零售外汇牌照79.67
- 监管中GTCFX10-15年 | 阿联酋监管 | 毛里求斯监管 | 瓦努阿图监管60.85
- 监管中VSTAR塞浦路斯监管| 直通牌照(STP)80.00
- 监管中IC Markets10-15年 | 澳大利亚监管 | 塞浦路斯监管91.81
- 监管中markets4you毛里求斯监管| 零售外汇牌照| 主标MT4| 全球展业|75.06
- 监管中CPT Markets Limited5-10年 | 英国监管 | 伯利兹监管91.56


